Edle und unedle Metalle
Zielsetzung: Das Arbeitsblatt vermittelt die chemische Unterscheidung zwischen edlen und unedlen Metallen. Die Lernenden sollen die Zusammenhänge zwischen der Stellung im Periodensystem, der Elektronenabgabe (Ionisierungsenergie) und der Reaktionsbereitschaft verstehen sowie die praktische Anwendung der elektrochemischen Spannungsreihe erlernen.
Inhalte und Methoden: Die Inhalte werden durch die Kombination aus theoretischen Grundlagen, Tabellenanalyse und experimenteller Überprüfung vermittelt: Zunächst werden edle und unedle Metalle anhand ihrer Reaktivität, Beständigkeit und Stellung in der chemischen Spannungsreihe mit Standardpotentialen unterschieden. Anschließend vertiefen die Lernenden ihr Verständnis durch Experimente zur Verdrängungsreaktion und zur Beständigkeit. Die systematische Dokumentation der Beobachtungen sowie Transferaufgaben sichern das Fachwissen und fördern die Anwendung auf weitere Metallvergleiche.
Kompetenzen:
- Fachkompetenz: Einordnung von Metallen in die Spannungsreihe und Verständnis des Redox-Begriffs (Elektronenabgabe/-aufnahme)
- Erkenntnisgewinnung: Planung und Durchführung von Experimenten zur Reaktivitätsprüfung unter Einhaltung von Sicherheitsstandards (H- und P-Sätze)
- Analysefähigkeit: Verknüpfung von stofflichen Veränderungen (Belag, Farbe) mit chemischen Gesetzmäßigkeiten
Zielgruppe und Niveau: Ab Klasse 9
50 other teachers use this template
Target group and level
ab Klasse 9
Subjects
Edle und unedle Metalle
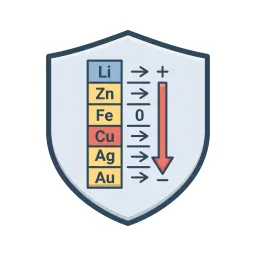
Einstieg und Grundbegriffe
- Lies dir den Informationstext über die Einteilung von Metallen in edle und unedle aufmerksam durch.
- Nutze dieses Wissen, um die folgende Tabelle zu typischen Eigenschaften wie Korrosionsanfälligkeit korrekt auszufüllen.
Edle und unedle Metalle
Metalle kann man in edle und unedle Metalle einteilen. Diese Unterscheidung hilft, ihr Verhalten in der Chemie besser zu verstehen.
Edle Metalle reagieren nur sehr wenig mit Sauerstoff, Wasser oder anderen Stoffen aus ihrer Umgebung. Sie bleiben lange glänzend und laufen kaum an. Man verwendet sie häufig für Schmuck, Münzen oder besondere technische Geräte, weil sie schön aussehen und sehr beständig sind. Chemisch gesehen geben edle Metalle ihre Elektronen nur schwer ab. Sie haben hohe Ionisierungsenergien und stehen im Periodensystem eher weiter rechts.
Unedle Metalle reagieren dagegen leicht mit Sauerstoff und Wasser. Sie werden schnell matt, rosten oder bilden andere Verbindungen auf ihrer Oberfläche. Das Aussehen verändert sich deutlich, zum Beispiel durch Rost oder eine trübe Schicht. Unedle Metalle geben in chemischen Reaktionen ihre Elektronen leicht ab. Sie besitzen niedrigere Ionisierungsenergien und stehen im Periodensystem meist weiter links.
Der wichtigste Unterschied zwischen edlen und unedlen Metallen liegt also in ihrer Reaktionsbereitschaft und in ihrer Fähigkeit, Elektronen abzugeben. Edle Metalle sind chemisch stabil, reagieren kaum und behalten ihren Glanz. Unedle Metalle sind reaktionsfreudig, korrosionsanfällig und verändern ihr Aussehen schneller.
Dieser Unterschied spielt in Technik und Alltag eine große Rolle. Beim Bau von Maschinen, Fahrzeugen oder Gebäuden muss man wissen, welche Metalle schnell rosten und geschützt werden müssen. Bei der Herstellung von Schmuck wählt man dagegen Metalle, die lange schön bleiben und nicht leicht anlaufen.
Eigenschaften von Metallen
| Eigenschaft | Unedle Metalle | Edle Metalle |
|---|---|---|
| reaktionsträge | ||
| reaktionsfreudig | ||
| stabil | ||
| korrosionsanfällig | ||
| gibt leicht Elektronen ab | ||
| gibt schwer Elektronen ab |
Vertiefung und Spannungsreihe
- Analysiere die Tabelle zur chemischen Spannungsreihe und vergleiche die verschiedenen Redox-Paare.
- Beantworte auf dieser Grundlage die Transferfragen, um zu bestimmen, welches Metall jeweils „unedler“ ist oder leichter Elektronen abgibt.
Redox-Paare und Standardpotentiale
| Element im Redox-Paar | oxidierte Form | + z e− ⇌ | reduzierte Form | Standardpotential E° |
|---|---|---|---|---|
| Magnesium (Mg) | Mg2+ | + 2 e− ⇌ | Mg | −2,362 V |
| Kupfer (Cu) | Cu2+ | + 2 e− ⇌ | Cu | +0,339 V |
| Zink (Zn) | Zn2+ | + 2 e− ⇌ | Zn | −0,762 V |
| Aluminium (Al) | Al3+ | + 3 e− ⇌ | Al | −1,677 V |
| Eisen (Fe) | Fe2+ | + 2 e− ⇌ | Fe | −0,41 V |
| Blei (Pb) | Pb2+ | + 2 e− ⇌ | Pb | −0,126 V |
| Silber (Ag) | Ag+ | + 2 e− ⇌ | Ag | +0,799 V |
| Gold (Au) | Au3+ | + 3 e− ⇌ | Au | +1,498 V |
| Wasserstoff (H) | 2 H+ | + 2 e− ⇌ | H2 | 0 V |
Experimentelle Untersuchung
Gruppenarbeit
- Bildet Gruppen aus jeweils vier Personen.
- Verteilt die Aufgaben sinnvoll (z. B. Durchführung, Protokoll, Material, Beobachtung).
- Arbeitet während der gesamten Experimente eng zusammen.
Vor jedem Experiment
- Lest die Versuchsanleitung genau durch.
- Beachtet alle Sicherheitsvorgaben.
- Stellt sicher, dass jedes Gruppenmitglied alles verstanden hat.
Wichtiger erster Schritt
- Bearbeitet die erste Aufgabe vor jedem Experiment.
- Sie hilft euch, die Versuche besser zu verstehen und richtig durchzuführen.
Durchführung
- Nutzt euer Wissen über:
- edle und unedle Metalle
- Spannungsreihe
- Untersucht die vorgegebenen Metalle
Beobachtung
- Achtet besonders auf:
- Farbänderungen
- Bildung von Gasen
- Diese Hinweise sind wichtig.
Dokumentation
- Haltet alle Ergebnisse sorgfältig fest:
- Beobachtungen
- Auswertungen (2. + 3. Aufgabe)
Experiment: Nachweis der unedlen Eigenschaft von Magnesium mit Kupfersulfatlösung
Materialien:
1 Becherglas (100 ml), 1 Pinzette, 1 Stück Küchenpapier, Schutzbrille, Schutzhandschuhe, Laborkittel
Chemikalien:
Kupfersulfatlösung (CuSO₄, c = 0,1 mol/l, wässrige Lösung)
H-Sätze: H302, H315, H319
P-Sätze: P280, P305+P351+P338, P301+P312
Magnesiumband
Hinweise zur Sicherheit:
• Trage immer Schutzbrille, Schutzhandschuhe und Laborkittel.
• Fasse Chemikalien niemals mit den Händen an.
• Iss und trinke nicht im Chemieraum.
• Probiere niemals Chemikalien. Nimm nichts in den Mund.
• Vermeide den Kontakt der Lösung mit Haut, Augen und Kleidung.
• Wenn Lösung auf die Haut oder in die Augen kommt, spüle sofort mit viel Wasser und informiere sofort die Lehrkraft.
• Halte das Gesicht von den Gefäßen fern.
Durchführung:
- Setze deine Schutzbrille auf und ziehe Schutzhandschuhe und Laborkittel an.
- Gib mit Hilfe der Lehrkraft 50 ml Kupfersulfatlösung in das Becherglas.
- Nimm das Magnesiumband mit der Pinzette und reinige es, falls nötig, vorsichtig mit einem Tuch (nicht mit den Fingern).
- Lege das etwa 5 cm lange Magnesiumband mit der Pinzette vorsichtig in die Kupfersulfatlösung.
- Stelle das Becherglas ruhig auf den Tisch und warte etwa 10 Minuten.
- Beobachte in dieser Zeit genau das Magnesiumband und die Lösung:
- Achte auf die Farbe des Magnesiumbandes.
- Achte auf Veränderungen der Oberfläche (Belag, Farbe).
- Achte auf die Farbe der Lösung.
- Achte darauf, ob sich Gasbläschen bilden.
- Nimm nach der Beobachtungszeit das Magnesiumband mit der Pinzette aus der Lösung.
- Lege das Magnesiumband auf ein Stück Küchenpapier und lasse es trocknen.
- Entsorge die Lösung nach den Anweisungen der Lehrkraft.
Arbeitsauftrag:
- Überlege vor dem Experiment, warum ein unedles Metall ein anderes Metall aus einer Lösung verdrängen kann.
- Beobachte während des Experiments genau, wie sich das Aussehen des Magnesiumbandes und die Farbe der Lösung verändern.
- Notiere nach dem Experiment, was die Veränderungen am Magnesiumband und in der Lösung über die Reaktivität von Magnesium im Vergleich zu Kupfer zeigen.
Experiment: Nachweis der edlen Eigenschaft von Kupfer mit Salzsäure
Materialien:
1 Becherglas (100 ml), 1 Pinzette, 1 Stück Kupferblech, Schutzbrille, Schutzhandschuhe, Küchenpapier
Chemikalien:
Salzsäure (HCl, wässrige Lösung, c = 1 mol/l)
H-Sätze: H290, H314, H335
P-Sätze: P280, P301+P330+P331, P305+P351+P338
Hinweise zur Sicherheit:
• Trage immer Schutzbrille und Schutzhandschuhe.
• Fasse Chemikalien niemals mit den Händen an.
• Vermeide das Einatmen von Dämpfen.
• Iss und trinke nicht im Chemieraum.
• Vermeide den Kontakt mit Haut, Augen und Kleidung.
• Sollte Salzsäure auf deine Haut oder in deine Augen gelangen, spüle sofort mit viel Wasser und informiere eine Lehrkraft.
• Verkoste niemals Chemikalien oder Lösungen.
Durchführung:
- Setze deine Schutzbrille und Schutzhandschuhe auf.
- Gib mit Hilfe der Lehrkraft etwa 50 ml Salzsäure in das Becherglas.
- Nimm das Kupferblech mit der Pinzette und lege es vorsichtig in die Salzsäure.
- Beobachte das Kupferblech und die Lösung für mindestens 10 Minuten.
- Achte dabei besonders darauf, ob sich Bläschen bilden, ob sich die Farbe der Lösung verändert oder ob sich das Aussehen des Kupferblechs ändert.
- Nimm nach der Beobachtungszeit das Kupferblech mit der Pinzette aus der Lösung.
- Spüle das Kupferblech mit Wasser ab und lege es auf Küchenpapier zum Trocknen.
- Entsorge die Salzsäurelösung nach den Anweisungen der Lehrkraft.
Arbeitsauftrag:
- Überlege vor dem Experiment, warum du erwartest, dass Kupfer sich in Salzsäure entweder auflöst oder nicht auflöst.
- Beobachte während des Experiments genau, ob sich Bläschen bilden, ob sich die Lösung verfärbt oder ob sich das Kupferblech sichtbar verändert.
- Notiere nach dem Experiment, was deine Beobachtungen über die Reaktivität von Kupfer in verdünnter Salzsäure aussagen.
Lösung für die Lehrkraft
Reaktionsträge – edle Metalle
- Reagieren kaum mit Sauerstoff und Wasser
- Bleiben lange glänzend und laufen nicht schnell an
Reaktionsfreudig – unedle Metalle
- Reagieren leicht mit Sauerstoff und Wasser
- Bilden schnell Rost oder andere Verbindungen
Stabil – edle Metalle
- Sind chemisch beständig
- Verändern ihr Aussehen kaum und korrodieren wenig
Korrosionsanfällig – unedle Metalle
- Rosten schnell oder bilden trübe Schichten
- Müssen oft geschützt werden (z. B. Lack, Beschichtung)
Gibt leicht Elektronen ab – unedle Metalle
- Haben niedrigere Ionisierungsenergien
- Reagieren deshalb schneller und stärker
Gibt schwer Elektronen ab – edle Metalle
- Haben hohe Ionisierungsenergien
- Reagieren wenig und bleiben deshalb lange unverändert