
Luftzusammensetzung und Schadstoffe
Zielsetzung: Das Arbeitsblatt vermittelt die chemischen Grundlagen der Erdatmosphäre und sensibilisiert für die Gefahren durch Schadstoffe. Die Lernenden sollen die Anteile der verschiedenen Gase kennenlernen, das Teilchenmodell auf Gase anwenden und die lebensfeindlichen Bedingungen anderer Planeten (Mars) mit der Erde vergleichen.
Inhalte und Methoden: Die Inhalte werden durch den Vergleich von Daten, grafische Darstellungen und modellhaftes Denken vermittelt: Ausgehend von einem kontrastierenden Einstieg werden die Zusammensetzung der Luft sowie die Eigenschaften ihrer Hauptbestandteile erarbeitet und mithilfe eines Diagramms visualisiert. Darauf aufbauend erfolgt ein Vergleich unterschiedlicher Atmosphären sowie die Analyse eines ausgewählten Schadstoffs hinsichtlich Ursachen und Folgen. Abschließend wird das Verständnis durch die Einführung eines Teilchenmodells zur Beschreibung der Luft vertieft.
Kompetenzen:
- Fachwissen: Kenntnis der Haupt- und Spurengase der Luft und deren Funktionen
- Modellkompetenz: Anwendung des Teilchenmodells zur Erklärung nicht sichtbarer Gasgemische und deren Veränderung durch Schadstoffe
- Bewertungskompetenz: Beurteilung der Luftqualität und Verständnis der globalen Auswirkungen von Schadstoffemissionen auf Gesundheit und Klima
Zielgruppe und Niveau: Ab Klasse 8
BNE:
- SDG 13 (Maßnahmen zum Klimaschutz): Verständnis der Rolle von Treibhausgasen für das globale Klima
50 other teachers use this template
Target group and level
ab Klasse 8
Subjects
Luftzusammensetzung und Schadstoffe

Einstieg
Du bist Umwelt-Analytiker:in und untersuchst zwei Orte: eine Industrieanlage und einen Stadtwald.
- Schau dir die Karikatur genau an.
- Überlege: An welchem Ort gibt es mehr „unsichtbare Gäste“ (Schadstoffe) in der Luft?
- Begründe deine Meinung kurz (1–3 Sätze).
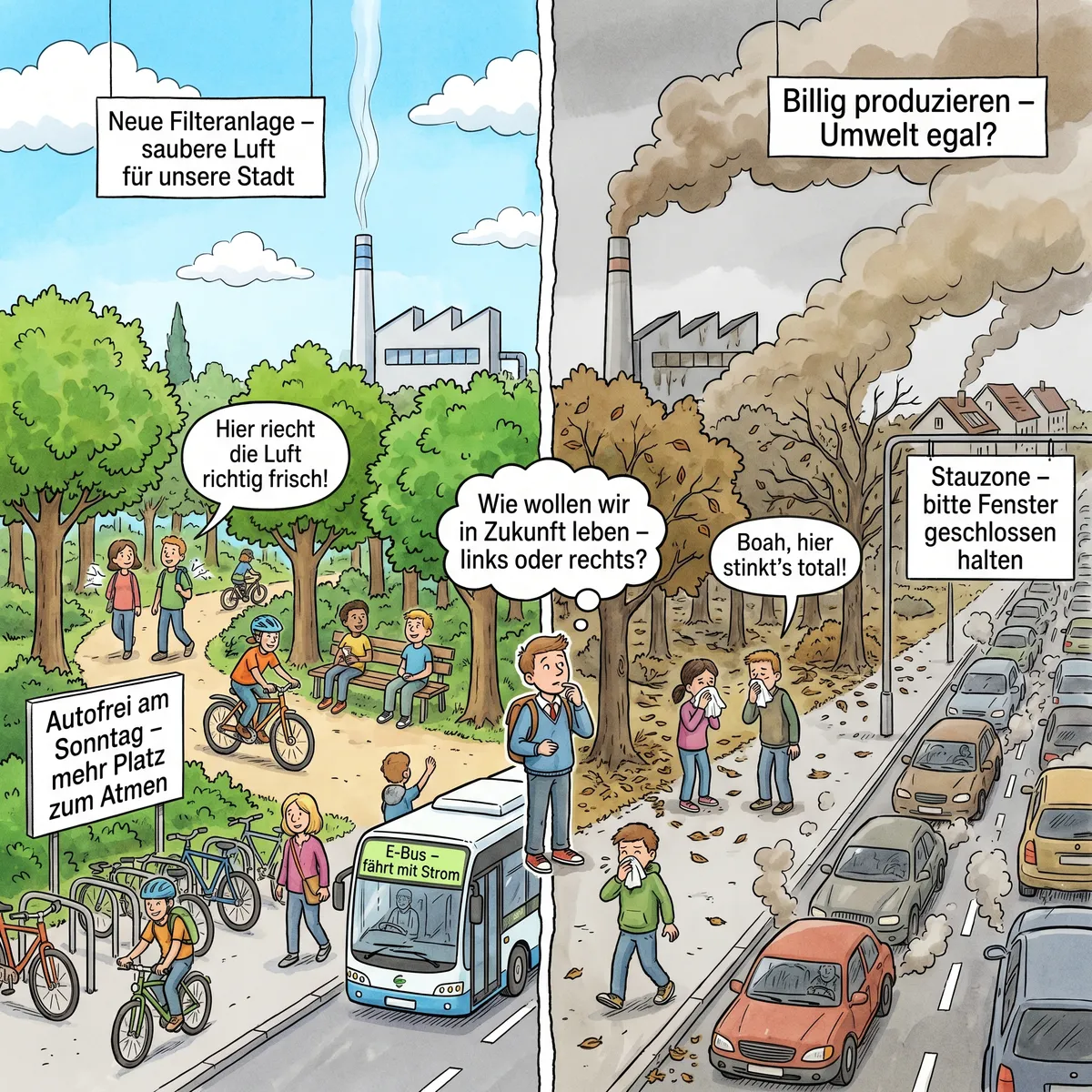
Wo vermutest du mehr 'unsichtbare Gäste' in der Luft? Begründe kurz.
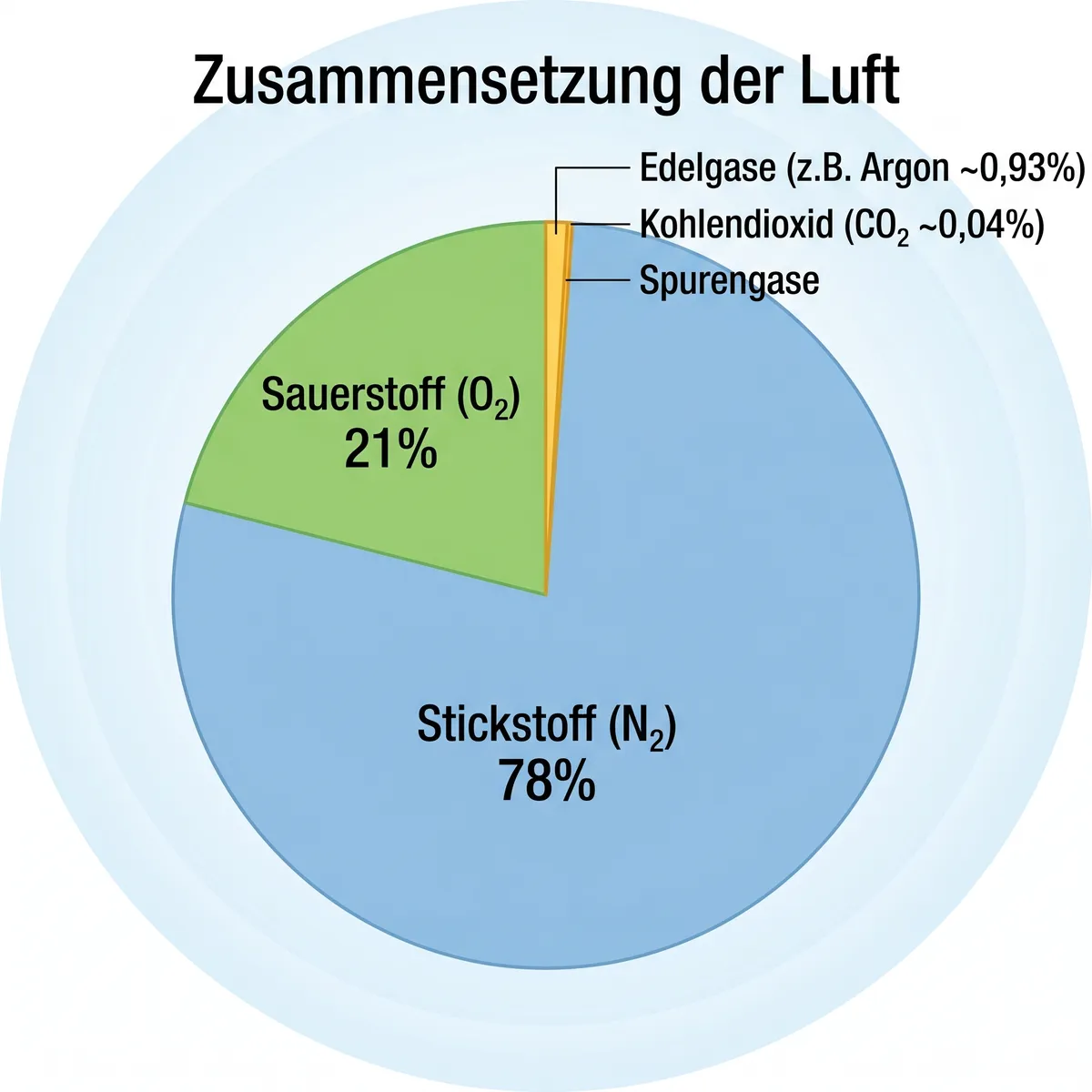
Die Zusammensetzung der Luft
Lies dir die Luftzusammensetzung genau durch.
Zeichne ein leeres Tortendiagramm und schreibe die Namen der Gase und die Prozentzahlen an die richtigen "Tortenstücke".
Lade Zeichenfeld...
Lösung für die Lehrkraft
Schadstoffe in der Luft – Im Fokus: Stickstoffdioxid
Die Luft, wie du schon weißt, besteht hauptsächlich aus den Gasen Stickstoff und Sauerstoff. Neben diesen natürlichen Bestandteilen gibt es jedoch auch sogenannte Schadstoffe, die durch menschliche Aktivitäten oder natürliche Prozesse in die Luft gelangen. Ein besonders wichtiger Schadstoff ist das Stickstoffdioxid (NO₂).
Was ist Stickstoffdioxid?
Stickstoffdioxid ist ein Gas, das zur Gruppe der Stickstoffoxide gehört. Es entsteht vor allem, wenn fossile Brennstoffe wie Kohle, Öl oder Gas verbrannt werden. Das passiert zum Beispiel in Autos, Fabriken oder Heizkraftwerken. Chemisch setzt sich Stickstoffdioxid aus einem Stickstoffatom (N) und zwei Sauerstoffatomen (O₂) zusammen. Die Formel dafür ist NO₂.
Im Gegensatz zu Stickstoff, dem Hauptbestandteil der Luft, ist Stickstoffdioxid kein ungefährlicher „Füllstoff“. Stickstoff selbst ist farb- und geruchlos sowie sehr reaktionsträge – das heißt, er geht kaum chemische Reaktionen ein. Stickstoffdioxid hingegen ist ein braun-gelbes Gas mit stechendem Geruch und sehr reaktiv. Es kann leicht mit anderen Stoffen reagieren und dadurch schädliche Verbindungen bilden.
Warum ist Stickstoffdioxid schädlich?
Stickstoffdioxid ist ein Schadstoff, weil es sowohl für Menschen als auch für die Umwelt gefährlich sein kann. Wenn wir NO₂ einatmen, reizt es die Atemwege und kann Husten, Atemnot oder sogar Asthma verursachen. Besonders Kinder, ältere Menschen und Menschen mit Atemwegserkrankungen sind gefährdet. In hohen Konzentrationen kann NO₂ sogar die Lunge schädigen.
Außerdem trägt NO₂ zur Bildung von sogenannten „sauren Regen“ bei. In der Atmosphäre reagiert NO₂ mit Wasser und Sauerstoff zu Salpetersäure (HNO₃). Diese gelangt mit dem Regen auf den Boden und kann Pflanzen, Tiere und Gebäude schädigen.
Unterschied zu den Hauptbestandteilen der Luft
Im Vergleich zu Stickstoff (N₂) und Sauerstoff (O₂) kommt Stickstoffdioxid nur in sehr geringen Mengen in der Luft vor. Während Stickstoff für Lebewesen in seiner normalen Form ungefährlich ist und Sauerstoff sogar lebensnotwendig, wirkt Stickstoffdioxid schon in kleinen Mengen schädlich. Das macht NO₂ zu einem echten Problemstoff, obwohl er mengenmäßig viel weniger vertreten ist als die Hauptbestandteile der Luft.
Chemische Eigenschaften und Bedeutung
Stickstoffdioxid ist ein sogenanntes „reaktives Gas“. Das bedeutet, es kann leicht mit anderen Stoffen chemische Reaktionen eingehen. Das unterscheidet es deutlich von Stickstoff oder den Edelgasen in der Luft, die fast gar nicht reagieren. Durch seine hohe Reaktivität kann NO₂ in der Atmosphäre weitere Schadstoffe, wie zum Beispiel Ozon (O₃), mitbilden. Ozon in Bodennähe ist ebenfalls schädlich für die Gesundheit.
Zusammenfassung
Stickstoffdioxid ist ein Luftschadstoff, der durch Verbrennungsvorgänge entsteht. Im Gegensatz zu den Hauptbestandteilen der Luft ist NO₂ schon in kleinen Mengen gefährlich. Es reizt die Atemwege, schadet der Umwelt und ist chemisch sehr reaktionsfreudig. Deshalb ist es wichtig, die Menge an Stickstoffdioxid in der Luft möglichst gering zu halten und Maßnahmen zum Umweltschutz zu unterstützen.
Schadstoffe gefunden
Lies dir den Informationstext genau durch und fülle mit dem gewonnen Wissen den Steckbrief aus.
Beantworte anschließend die folgenden Fragen.
Ein internationales Forscherteam vergleicht die Luft der Erde mit der des Mars, um herauszufinden, welche Rolle Stickstoffdioxid (NO₂) spielt. Auf der Erde entsteht dieses Gas vor allem bei der Verbrennung von fossilen Brennstoffen in Autos, Heizkraftwerken und Industrieanlagen. Dort mischt es sich als kleiner, aber gefährlicher Bestandteil unter die übrigen Luftgase. Wegen seiner hohen Reaktivität verbindet sich NO₂ leicht mit Wasser und Sauerstoff zu Salpetersäure, was zu saurem Regen führt und Wälder, Böden sowie Gebäude schädigen kann. Beim Einatmen reizt NO₂ die Atemwege, löst Husten und Atemnot aus und kann langfristig die Lunge schädigen.
Auf dem Mars finden die Forschenden eine völlig andere Situation vor. Die Atmosphäre besteht dort fast vollständig aus Kohlendioxid (CO₂), während Stickstoff und Sauerstoff nur in Spuren vorkommen. NO₂ wird auf dem Mars nicht durch Verkehr oder Industrie erzeugt, sondern höchstens in winzigen Mengen durch Blitze in Staubstürmen oder kosmische Strahlung. Wegen der extrem dünnen Luft und der sehr niedrigen Temperaturen kann sich dieses Gas kaum anreichern, sodass seine Wirkung auf mögliche Umweltschäden gering bleibt. Dennoch wäre NO₂ für Astronaut:innen in Marsstationen ein ernstes Problem: Gelangt es in geschlossene Lebensräume, würde seine chemische Formel NO₂ anzeigen, dass schon kleine Konzentrationen ausreichen, um Schleimhäute zu reizen und technische Materialien anzugreifen. So zeigt der Vergleich, dass derselbe Stoff auf zwei Planeten völlig unterschiedliche Bedeutungen haben kann.

Infobox: Wie Chemiker:innen denken – Das Teilchenmodell
Da wir Gase nicht sehen können, nutzen Chemiker:innen ein Modell. Ein Modell ist eine Idee, die hilft, Beobachtungen zu erklären.
Wichtige Prinzipien des Teilchenmodells bei Gasen:
- Teilchen und Leere: Gase bestehen aus winzigen Teilchen. Zwischen diesen Teilchen ist absolut nichts (leerer Raum).
- Abstand: Die Teilchen sind sehr weit voneinander entfernt.
- Dauerhafte Bewegung: Die Teilchen bewegen sich ständig und völlig ungeordnet in alle Richtungen.
- Geschwindigkeit: In der Luft bewegen sie sich mit ca. 330 m/s (fast Schallgeschwindigkeit!). Bei höherer Temperatur bewegen sie sich noch schneller.